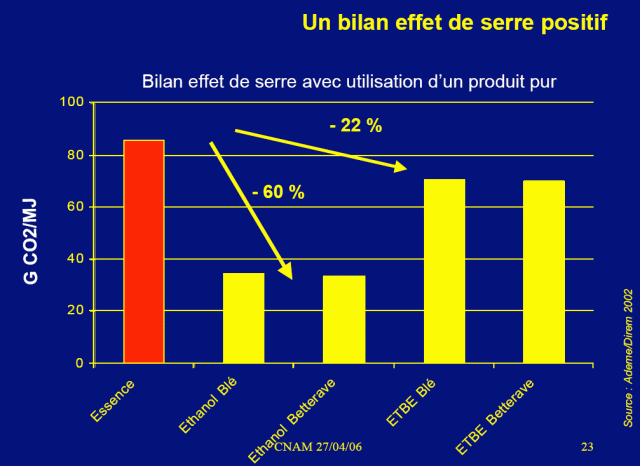
برای خروجی برابر موتور ، اتانول برای انجام کار مشابه ، 4,56 / 3,55 = 1,28/2 برابر بیشتر از بنزین CO تولید می کند.
به عبارت دیگر: اتانول 28٪ CO2 بیشتر از بنزین ساطع می کند.
و در این محاسبه برای اتانول محاسبه نمی شوند:
- هزینه های تولید CO2 گیاه غلات یا شکر
- هزینه های تصفیه گیاه به شکر
- هزینه های تقطیر
- هزینه های انرژی تخمیر (به عنوان مثال CO2 منتشر شده برای گرم کردن ملاس)
برخی از یادآوری های شیمی: شکر ، تخمیر ، الکل و CO2 ...
ما توده های اتمی زیر را که اساس تمام محاسبات است حفظ خواهیم کرد: C = 12 گرم در مول ، O = 16 گرم در مول ، H = 1 گرم در مول
الف) مورد الكل حاصل از تخمیر قند
شکر مورد استفاده در ساخت اتانول از خانواده دی هولوزیدها (ساکارز یا مالتوز) فرمول: C12H22O11 (نگاه کنید به http://fr.wikipedia.org/wiki/Sucre#Chimie ) دارای جرم مولی 342 گرم است که با هیدرولیز (یک مولکول آب "به دست می آورد") ، 2 مولکول گلوکز یا 2 * C6H12O6 با وزن مولر 180 گرم برای جرم کل 360 را به شما می دهد. گرم
جزئیات گلوکز: http://fr.wikipedia.org/wiki/Glucose
سپس مول گلوکز طبق معادله تخمیر می شود:
کد: را انتخاب کنید
C6H12O6 --> 2*C2H6O + 2*CO2محصولات: 2 مول الکل اتیل (C2H6O = 46 گرم در مول) و دو مول دی اکسید کربن (CO2 = 44 گرم در مول).
قبل از سوختن و نادیده گرفتن هرگونه انتشار دیگر CO2 ، بنابراین هر گرم الکل تولید شده در حین "ایجاد" آزاد می شود: 44/46 = 0.95 گرم CO2.
و این قبل از احتراق آن است. در طی احتراق الکل:
کد: را انتخاب کنید
C2H6O + 7/2*O2 --> 2*CO2 + 3*H2O یا برای کسانی که اعداد گرد را ترجیح می دهند:
کد: را انتخاب کنید
2*C2H6O + 7*O2 --> 4*CO2 + 6*H20خطای تعادل در معرف ها ، اقدام اصلاحی (که نتایج را در CO2 تغییر نمی دهد):
کد: را انتخاب کنید
C2H6O + 3*O2 --> 2*CO2 + 3*H2O با سوزاندن ، این خال 46 گرم الکل 88 گرم CO2 (2 مول) تولید می کند.
بنابراین ما در مجموع 3 مول CO2 ساطع شده در هر مول الکل سوخته به دست می آوریم: 1 در هنگام تخمیر و 2 در هنگام احتراق. بنابراین در کل 3x44 = 132 گرم CO2 برای 46 گرم الکل سوخته.
نتیجه گیری: بنابراین هر گرم الکل در حین تولید و احتراق خود حداقل 132/46 = 2,87/2 گرم COXNUMX ساطع می کند.
حداقل می گویم زیرا بسیاری از "موقعیت های CO2" مورد توجه قرار نگرفته اند: تولید شکر و تقطیر الکل بدون شک بیشترین مصرف انرژی را دارند.
بنابراین این مقدار 2,87 گرم CO2 / گرم الکل مقدار بسیار کمی است!
ب) مورد بنزین (که الکل قرار است جایگزین آن شود)
من بدون جزئیات محاسبات در این صفحه از سر می گیرم: معادلات احتراق و CO2
انتشار CO2 برای هیدروکربن فرمول C2H (2n + 2) = 44n
کاربرد روی بنزین (اکتان خالص). n = 8
[C8H18] = 8 12 * + = 18 1 114 * گرم / مول.
جرم CO2 آزاد شده به ازای هر مول اکتان مصرف شده: 44 * 8 = 352 گرم است.
نسبت مصرف بنزین به انتشار CO2 352/114 = 3,09 است
نتیجه گیری: بنابراین هر گرم بنزین 3,09 گرم CO2 در هنگام احتراق منتشر می کند
هزینه "پالایش" در بدترین حالت 15٪ ، 3.55 گرم CO2 برای تصفیه و احتراق بنزین بدست می آورد.
ج) مقایسه انرژی اتانول و بنزین
کد: را انتخاب کنید
PCI ethanol = 26 900 kJ/kg
PCI essence = 42 700 kJ/kg
بنابراین در بازده موتور ، 42,7 / 26,9 = برابر جرم اتانول بیشتر برای تأمین انرژی مشابه ، 1,59 برابر زمان لازم است.
در ایزو انرژی ، بنابراین لازم است ضریب 1,59 به میزان انتشار CO2 اتانول اضافه شود: بنابراین 2,87 گرم به 4,56 گرم تبدیل می شود. و به یاد داشته باشید: این 2,87 گرم قبلاً بسیار کاهش یافته بود زیرا کشت قند را در نظر نگرفتند (اما افراد مشکوک با دلیل می گویند که برای بنزین ، ما هزینه های استخراج و حمل و نقل نفت خام)
نتیجه گیری کلی
برای تأمین همان مقدار انرژی احتراق ، میزان انتشار CO2 به ترتیب عبارتند از:
- با بنزین: 3,55 گرم CO2
- با اتانول: 4,56 گرم CO2
برای خروجی برابر موتور ، اتانول برای انجام کار مشابه ، 4,56 / 3,55 = 1,28/2 برابر بیشتر از بنزین CO تولید می کند.
به عبارت دیگر: اتانول 28٪ CO2 بیشتر از بنزین ساطع می کند.
و در این محاسبه برای اتانول محاسبه نمی شوند:
- هزینه های تولید CO2 گیاه غلات یا شکر
- هزینه های تصفیه گیاه به شکر
- هزینه های تقطیر
- هزینه های انرژی تخمیر (به عنوان مثال CO2 منتشر شده برای گرم کردن ملاس)
بنابراین شکی وجود ندارد: با توجه به این استدلال ، اتانول منشا sugar قند کشاورزی بسیار بیشتر از بنزین CO2 منتشر می کند. بنابراین چگونه سازمان های ایالتی و دانشگاه ها می توانند چنین ارزیابی های مثبت CO2 در مورد اتانول بدست آورند؟ آیا تخمیر را در نظر نمی گیرند؟ چه چیزی را از دست می دهند؟ یا نقص در استدلال ما کجاست؟